Чтобы найти решение, как увеличить успешность ЭКО, нужно знать и понимать причины неудач ЭКО.
Так сложилось, что в Международном Центре Фертильности мы помогаем пациентам с множественными неудачами ЭКО. Это началось еще в Российско-Финской клинике в Санкт-Петербурге, где до 2018 года работали Светлана Александровна Шлыкова, Ольга Геннадиевна Зайцева, Елена Николаевна Лапина, Алена Вячеславовна Егорова. К ним после множественных безуспешных попыток ЭКО приезжали пациенты со всей России, СНГ и Европы.
Традиция продолжилась и в Международном Центре Фертильности. Здесь к нам редко обращаются пациенты, которые делают ЭКО или инсеминацию впервые. Наши пациенты приходят или приезжают издалека, после многочисленных неудач ЭКО и потерь беременности, отчаявшиеся, потерявшие надежду на успех. Обычно мы знаем, как помочь: сначала дать поддержку, информацию, мотивацию и надежду, а потом распутать клубок неудач до самого его начала.
У наших пациентов обычно имеется более одной причины, почему беременность все еще не наступила. В противном случае первые попытки ЭКО по месту жительства уже привели бы к результату, и мы никогда бы не встретились.
Чтобы иметь возможность устранить или откорректировать каждую причину предыдущих неудач ЭКО, мы следуем принципу: “одна задача — одно решение”.
Этот подход известен уже давно: когда перед вами большой проект, вы разделяете его на меньшие проекты с промежуточными целями, которые все вместе приводят в итоге к конечной цели. В нашем случае промежуточными целями будут: получение яйцеклеток, получение бластоцист, получение бластоцист с нормальным набором хромосом, подготовленная матка, правильное окно имплантации и, наконец, - перенос бластоцисты с нормальным набором хромосом на подготовленный эндометрий в правильное время.
И наша конечная цель, конечно, это рождение ребенка.
Причины неудач ЭКО и потерь беременности можно разделить на две группы: эмбриональные и материнские.
Эмбриональные причины неудач ЭКО и потерь беременности кроются в самом эмбрионе. В силу этих внутренних причин эмбрион оказывается нежизнеспособным и не может развиваться в матке даже в самых комфортных условиях.
Материнские причины неудач ЭКО и потерь беременности кроются в организме женщины и могут препятствовать имплантации и развитию жизнеспособного эмбриона.
В этой главе мы остановимся на некоторых наиболее частых эмбриональных и материнских причинах неудач ЭКО и способах их устранения или корректировки.
I. Эмбриональные причины неудач ЭКО и потерь беременности

Рисунок 1. Кто отвечает за результат ЭКО: женщина или эмбрион?
Эмбриональные причины неудач ЭКО и потерь беременности оказывают огромное влияние на успех ЭКО и на 75% определяют результат ЭКО и исход беременности.
I.1. Генетические особенности эмбрионов человека
— У женщин после 35 лет эмбрионы часто имеют неправильный хромосомный набор [Fragouli et al., 2012] и, как бы странно это ни звучало, это является биологически обусловленной нормой.
— Неправильный набор хромосом эмбриона почти всегда приводит к потере беременности еще до имплантации (беременность не наступает) или после имплантации (спонтанное прерывание беременности) [Scott at al., 2012].
— Неправильный набор хромосом почти всегда материнского происхождения, т.е. эмбрион получает его из яйцеклетки.
— Чем старше яйцеклетка, тем больше вероятность того, что хромосомный набор эмбриона будет неправильным, и опять же, это биологическая норма.
— Влияние хромосомных аномалий на морфологию эмбриона (то, как эмбрион выглядит) на 5-6 день развития эмбриона, незначительно. Т.е. эмбрион может выглядеть красиво, но при этом иметь неправильный набор хромосом [Alfarawati et al., 2011].
Какая доля эмбрионов на стадии бластоцисты имеет нормальный набор хромосом?
Диаграмма 1. Доля бластоцист с нормальным набором хромосом у женщин разных возрастных групп по данным S. Munne et al:
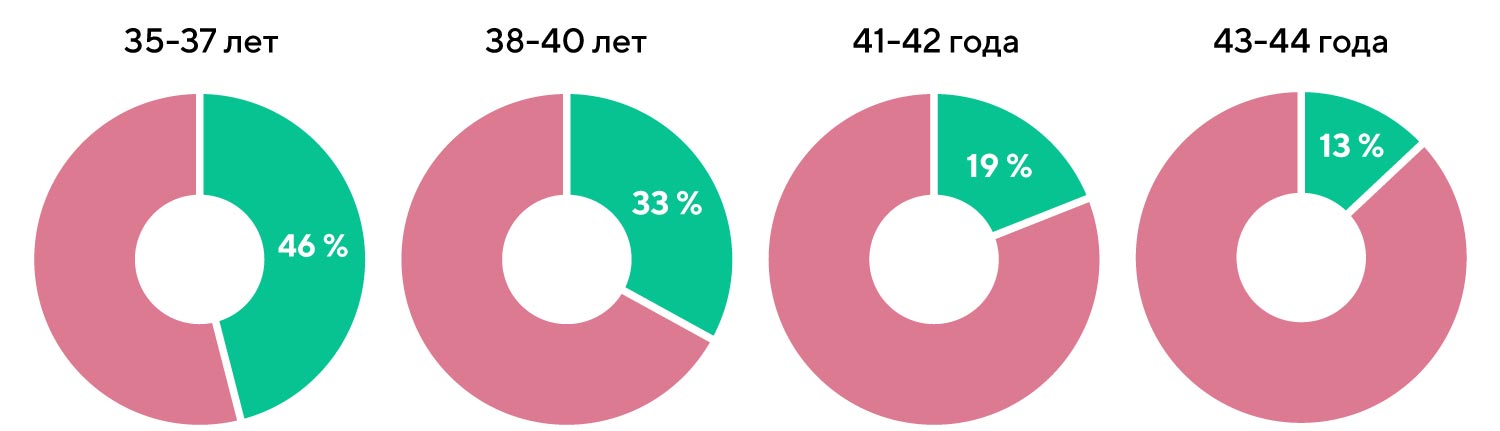
[S. Munne et al. Количество бластоцист, необходимое для переноса хотя бы одного эуплоидного эмбриона: данные 10 852 циклов преимплантационного генетического скрининга (ПГС). Fertility Sterility September 2015 Volume 104, Issue 3, Supplement, Pages e13–e14]
- Ожидается, что каждая вторая бластоциста будет иметь нормальный набор хромосом в возрастной группе 35-37 лет;
- Ожидается, что лишь одна из 8 бластоцист будет иметь нормальный набор хромосом к 43 годам.
Диаграмма 2. Доля бластоцист с нормальным набором хромосом у женщин разных возрастных групп по данным Международного Центра Фертильности с 2019 по 2022:

По данным Международного Центра Фертильности с 2019 по 2022 годы, доля бластоцист с нормальным набором хромосом в различных возрастных группах соответствует более раннему исследованию S. Munne et al.
I.2. ПГТ-А — преимплантационное генетическое тестирование эмбрионов
Есть ли способ определить, какие из бластоцист, имеющих нормальную морфологию (внешний вид), имеют и нормальный набор хромосом, а какие – нет?
Что такое ПГТ-A?
ПГТ-A — Преимплантационное генетическое тестирование на анеуплоидии (анеуплоидия — аномальное количество хромосом). Это генетическое исследование эмбрионов определяет, какие из полученных эмбрионов имеют нормальный набор хромосом. Исключив из использования эмбрионы с аномальным набором хромосом, мы увеличиваем частоту родов на каждый перенесенный эмбрион. Увеличение частоты родов на каждый перенос эмбриона происходит потому, что тестирование выявляет эмбрионы (с аномальным набором хромосом), которые приводят к потерям беременности, и в полость матки они не переносятся.
Какие задачи у ПГТ-A?
ПГТ-A не делает эмбрионы лучше. ПГТ-A помогает отобрать эмбрионы с нормальным набором хромосом из имеющихся, чтобы использовать их для переноса.
Как проводится ПГТ-A?
ПГТ-A определяет все 23 пары хромосом в ДНК эмбрионов. Эмбрионы с аномальным набором хромосом не приведут к рождению здорового ребенка, поэтому их исключают из использования. Для переноса в полость матки используются эмбрионы с нормальным набором хромосом.
Какие цели у ПГТ-A?
- Снизить частоту спонтанных потерь беременности.
- Увеличить частоту родов на один перенос эмбрионов.
- Сократить время до рождения ребенка (уменьшить количество переносов эмбрионов до наступления родов).
Что говорит статистика?
Диаграмма 3. STAR1 в сравнении с SART (Национальный отчет США 2014 - 2017 гг.) Исходы беременности

STAR — частота наступления прогрессирующей беременности на один перенос; обратите внимание, что все эти прогрессирующие на момент исследования беременности, уже привели к рождению детей
SART — частота родов на перенос одного эмбриона
Частота наступления родов в расчете на один перенос одного эмбриона после ПГТ-А в нашей клинике составляют 49%. Это означает, что в нашей клинике 49% переносов одного эмбриона с нормальным хромосомным набором приводят к рождению ребенка (Диаграмма 4).
Диаграмма 4. Частота наступления клинической беременности и частота наступления родов/прогрессирующей беременности в расчете на перенос эмбриона из собственных яйцеклеток, в зависимости от того, использовался метод ПГТ-А для проверки хромосомного статуса эмбриона или нет (данные переносов эмбрионов, осуществленных в 2020-2021).

Кому ПГТ-А помогает увеличить успех ЭКО?
У женщин в возрасте 35 лет и старше частота родов на один перенос эмбриона с нормальным набором хромосом (по данным ПГТ-A), значительно выше, чем в контрольной группе (без ПГТ-A). Также во многих случаях (спонтанные потери беременности, неудачи ЭКО) ПГТ-А увеличивает успех ЭКО у женщин до 35 лет.
Как происходит процесс биопсии эмбриона и ПГТ-A?
Рисунок 2. Процесс биопсии эмбриона

- С помощью пипетки эмбриолог проводит биопсию нескольких клеток из наружной клеточной массы эмбриона (будущей плаценты).
- Непосредственно после биопсии эмбриолог осуществляет индивидуальную криоконсервацию каждой бластоцисты.
- В генетической лаборатории из клеток эмбриональной плаценты получают ДНК и исследуют 23 пары хромосом, после чего дают ответ, какие эмбрионы содержат нормальный набор хромосом, а какие – нет.
- Эмбрионы с аномальным набором хромосом исключаются из использования в будущем.
- Эмбрионы с нормальным набором хромосом могут быть использованы для переноса в матку.
Появились вопросы?
II. Материнские причины неудач ЭКО и потерь беременности
Материнские причины неудач ЭКО и потерь беременности могут быть гормональной, воспалительной, иммунной природы. Причины могут быть связаны с состоянием органов репродуктивной системы или других органов и систем организма. Зачастую у наших пациентов имеется несколько причин, почему прогрессирующей беременности и родов еще не удалось достигнуть.
Мы подходим индивидуально к выявлению и коррекции причин неудач каждой пациентки, составляем индивидуальный маршрут от первой консультации до достижения цели – родов.
Ниже мы обсудим лишь наиболее частые причины неудач ЭКО, информация о которых может быть полезна многим пациентам.
II.1. Пропуск окна имплантации — одна из наиболее частых причин неудач в “свежих” циклах ЭКО
Процесс прикрепления эмбриона в матке называется имплантацией. Имплантация начинается с распознавания определенных рецепторов на поверхности эндометрия рецепторами на поверхности вышедшего из своей первоначальной оболочки эмбриона .
Окно имплантации — это временные рамки, в которые эти рецепторы присутствуют в эндометрии, обычно через 5-7 дней после начала выработки прогестерона овулировавшим фолликулом (желтым телом).
В норме в естественном цикле выработка прогестерона начинается со дня овуляции. Таким образом, обычно рецепторы на клетках эндометрия готовы к встрече с эмбрионом через 5-7 дней после овуляции. В то же время и эмбрион, осуществив процесс хэтчинга (вылупления из оболочки), готов к встрече с рецепторами эндометрия через 5-7 дней после овуляции — на 5-7 день своего развития
.
Природа очень мудро синхронизировала процессы подготовки эмбриона и эндометрия к имплантации:
- Эмбрион готов к имплантации через 5-7 дней после овуляции (Рисунок 3)
- Эндометрий готов к имплантации через 5-7 дней после овуляции (Рисунок 4)
Рисунок 3. Эмбрион готов к имплантации через 5-7 дней после овуляции
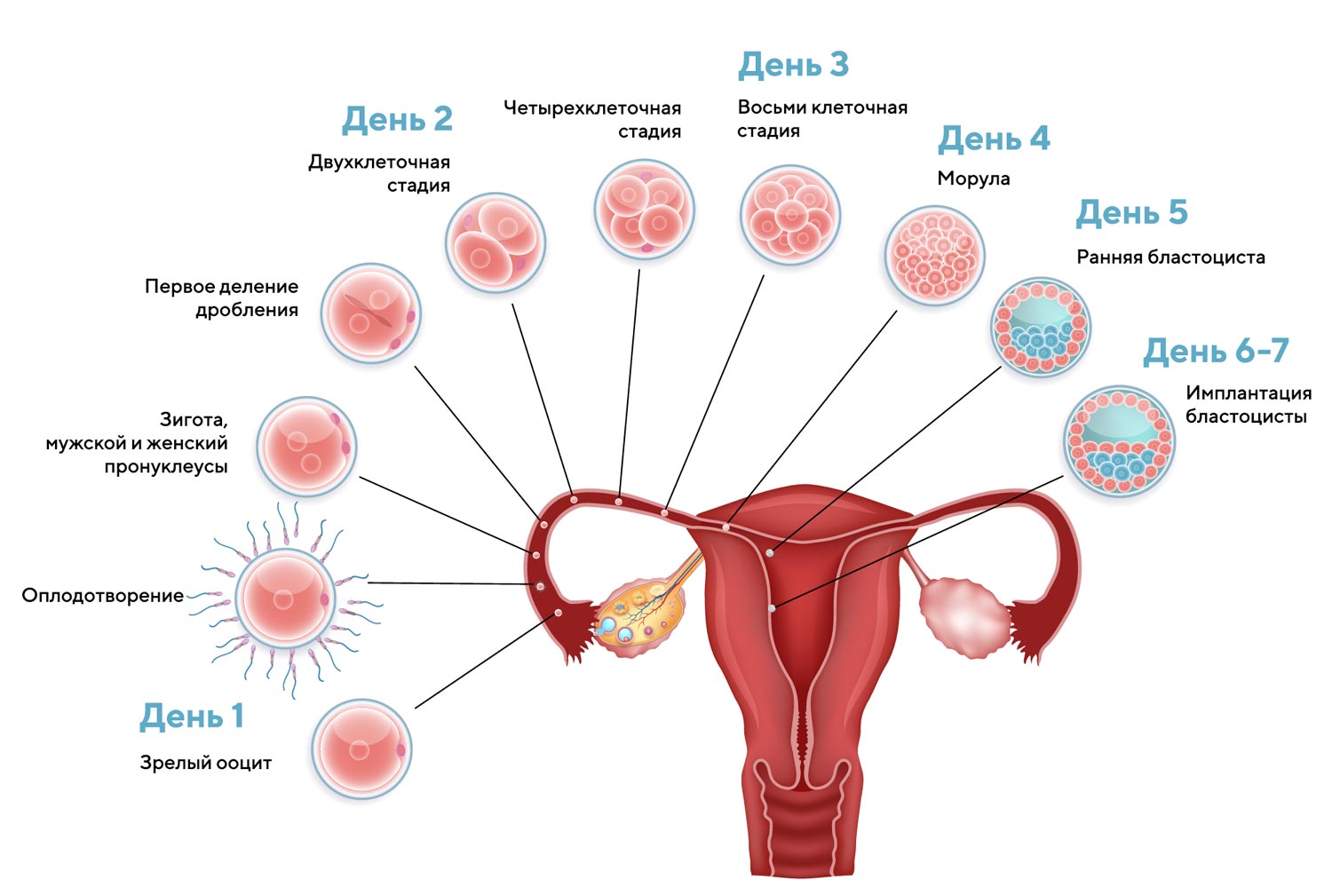
Рисунок 4. Эндометрий готов к имплантации через 5-7 дней после овуляции
 На Рисунке 4 изображено, как мудро природа синхронизировала процессы в яичниках и матке в естественном менструальном цикле
На Рисунке 4 изображено, как мудро природа синхронизировала процессы в яичниках и матке в естественном менструальном цикле
ФСГ стимулирует рост фолликулов с 4 по 14 день.
Фолликул (пузырек, содержащий яйцеклетку) растет и вырабатывает эстрогены.
Эстрогены стимулируют рост эндометрия в матке.
В ходе овуляции стенка фолликула разрывается, и яйцеклетка покидает его.
В норме выработка прогестерона начинается сразу после овуляции.
Прогестерон отвечает за то, чтобы сделать эндометрий способным к узнаванию эмбриона.
Обычно эндометрий готов к узнаванию и принятию эмбриона на 5-7 день после начала выработки прогестерона.
Продолжительность состояния готовности эндометрия узнать и принять эмбрион и является окном имплантации.
Именно момент начала выработки прогестерона определяет окно имплантации
Однако стимуляция яичников может рассинхронизировать эти 2 процесса: готовность эмбриона и эндометрия к имплантации. Это происходит, так как уровни половых гормонов во время стимуляции яичников многократно превышают естественные, характерные для натурального цикла. Во многих циклах стимуляции выработка прогестерона начинается слишком рано — еще за несколько дней до пункции фолликулов (пункция — эквивалент овуляции).
Если выработка прогестерона начнется раньше дня оплодотворения (пункции или дня овуляции), то рецепторы в эндометрии, которые могли бы распознать эмбрион, будут присутствовать там ранее того момента, когда сам эмбрион будет готов к имплантации. Когда же эмбрион достигнет стадии бластоцисты, готовой к имплантации, рецепторы в эндометрии, которые могли бы узнать эмбрион, могут уже отсутствовать, и этот диалог между эмбрионом и эндометрием будет невозможен. Эмбрион таким образом пропустил окно имплантации. Имплантация не состоится.
Рисунок 5. Рассинхронизация готовности эмбриона и эндометрия к имплантации является одной из наиболее частых причин нарушения имплантации в свежих циклах ЭКО

II.2. Пошаговое восстановление диалога между эмбрионом и маткой в процессе ЭКО
Нарушения диалога между эмбрионом и эндометрием можно избежать, если выполнять каждую задачу поэтапно.
Первым шагом является создание компетентных яйцеклеток и жизнеспособных эмбрионов при помощи индивидуально подобранного протокола стимуляции. Во время этой стимуляции мы должны сосредоточиться только на фолликулах, яйцеклетках и эмбрионах. Фокусироваться на эндометрии пока не представляется возможным.
Когда бластоцисты готовы, мы замораживаем их. Таким образом, мы можем переключить наше внимание на оптимальную подготовку матки к переносу эмбриона.
Для переноса эмбриона мы выбираем отдельный цикл, в котором сосредоточимся на эндометрии, чтобы перенести эмбрион на хорошо подготовленный эндометрий в оптимальное время. Обычно необходим один менструальный цикл после цикла стимуляции, чтобы яичники перестали вырабатывать остаточное количество прогестерона. Поэтому мы рекомендуем сделать перерыв в один цикл между циклом пункции и циклом переноса эмбриона.
Диаграмма 5. Кумулятивная частота наступления родов во всех группах пациентов, получивших переносы эмбрионов в рамках 1131 последовательного переноса эмбриона в Международном Центре Фертильности 2019-2021)

Ваши шансы в Международном Центре Фертильности:
- 51.6% шанс рождения ребенка после 1 переноса
- 75.4% шанс рождения ребенка после 2 переносов
- 85.6% шанс рождения ребенка после 3 переносов
- 88.9% шанс рождения ребенка после 4 переносов
Таким образом, если проявить настойчивость и последовательно двигаться к цели, шанс родить ребенка после 4 переносов эмбрионов в МЦФ составит 88.9%.
Вы хотите узнать больше?
ПОЗВОНИТЕ или напишите нам, и мы с радостью Вас проконсультируем

















